合成THC製剤「ナビロン(セサメット)」をパーキンソン病患者に6ヶ月間投与した結果、痛みや睡眠障害などの非運動症状が持続的に改善したことが報告されました。論文は「npj Parkinson’s Disease」に掲載されています。
パーキンソン病は主に安静時振戦、無動、筋強剛、姿勢保持異常などの運動障害をもたらす脳の病気(神経変性疾患)であり、日本では指定難病とされています。
パーキンソン病では運動障害だけではなく、過度な筋緊張・姿勢異常や自律神経の乱れなどにより、痛み、便秘、排尿障害、起立性低血圧、睡眠障害、抑うつ、不安などの「非運動症状」も認められます。
大麻やカンナビノイドは、主にECS(エンドカンナビノイドシステム)と呼ばれる神経系に作用することで医療効果をもたらすと考えられています。
様々な研究により、ECSとパーキンソン病との間には様々な関連性が指摘されています。そのため、ECSはパーキンソン病の治療標的としても注目されるようになっています。
THC製剤の長期的な有効性・安全性を検証
オーストリアのインスブルック医科大学の研究チームは以前、合成THC製剤「ナビロン(セサメット)」がパーキンソン病の非運動症状に有効なのかを検証するため、臨床試験(二重盲検ランダム化プラセボ対照試験)を実施。
ナビロン(ほどんどの患者が1mg/日で服用)を4週間投与した結果、プラセボと比較してパーキンソン病の非運動症状の悪化が抑制され、特に不安や睡眠障害において有効性が示されました。
今回の臨床試験はこれを拡張するものとなります。参加者は以前の研究において有効性を認め、中〜重度の副作用を経験しなかったパーキンソン病患者21名(平均年齢67.2歳、女性52.4%)。
ナビロンの服用は0.25mg/日からスタートし、2日目以降はこれを2回/日で服用。有効性が認められない、あるいは耐え難い副作用が出現しない限り、参加者は研究チームに報告の上、1〜4日おきに0.25mg増量することが可能でした。この増量期間は28日間であり、服用量は最大2mg/日までとされました。
増量期間の後、治験医師は3ヶ月おきに参加者と面会し、ナビロンの安全性及び有効性を評価。2回の面会(増量期間終了から3ヶ月後と6ヶ月後)が行われた後、参加者はナビロンの服用量を0.25mg/日ずつ減薬し、時間をかけて服用を中止。これに伴う影響についても評価が行われました。
忍容性は良好で、有効性も持続
解析対象に含まれた21名のうち、1名は睡眠障害、もう1名は元々認められていた軽度の認知障害が悪化したため、治療を中断。この2名を除いた19名の参加者が全ての治験を完了しました。
最も多く認められた副作用は集中力の低下(2名)でしたが、これはナビロンの服用量をわずかに減らすことで消失。重度な副作用、死亡、自殺は報告されず、認知障害(MMSE・MoCAのスコアに変化なし)、めまい、起立性低血圧といった副作用も観察されませんでした。
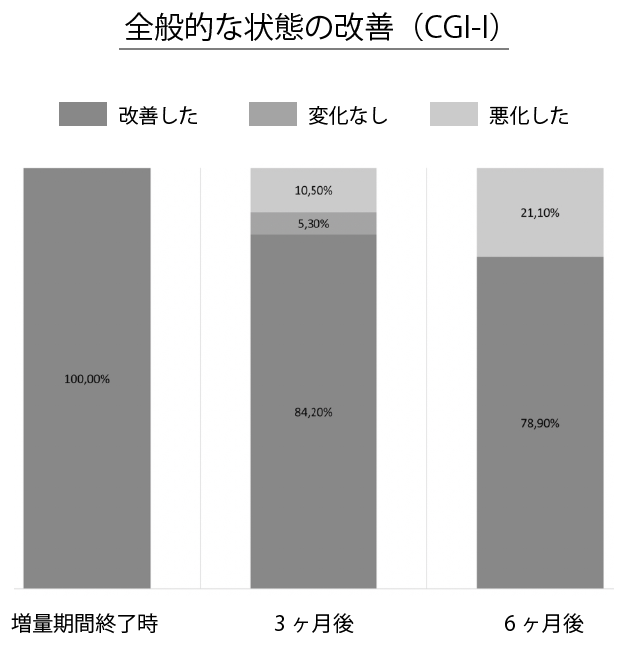
有効性に関しては、増量期間の終了時において参加者の全員が全般的な状態の改善(CGI-I)を報告。6ヶ月後では78.9%の患者において改善が持続しましたが、21.1%の患者では悪化が報告されました。
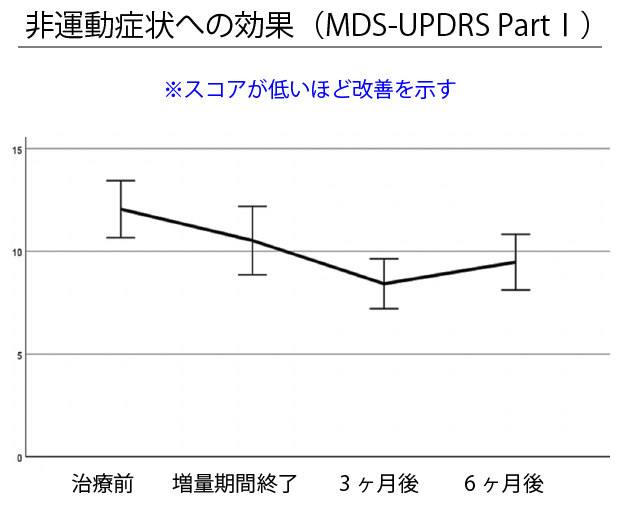
パーキンソン病の非運動症状は、治療開始前から適量摂取後6ヶ月目にかけて中程度改善(MDS-UPDRS PartⅠの平均スコア:-2.58点、効果量:-0.51)。特に、夜間の睡眠問題において大きな効果が観察されました(MDS-UPDRS1.7の平均スコア:-1.42、効果量:-0.92)。
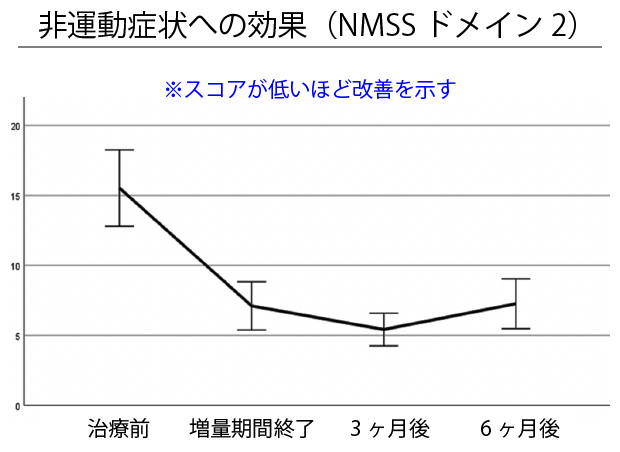
別の非運動症状の評価(NMSS)でも同様に、睡眠・疲労の領域(ドメイン2)において有意な改善が示されました(NMSSドメイン2の平均スコア:-8.26点、効果量:-0.72)。
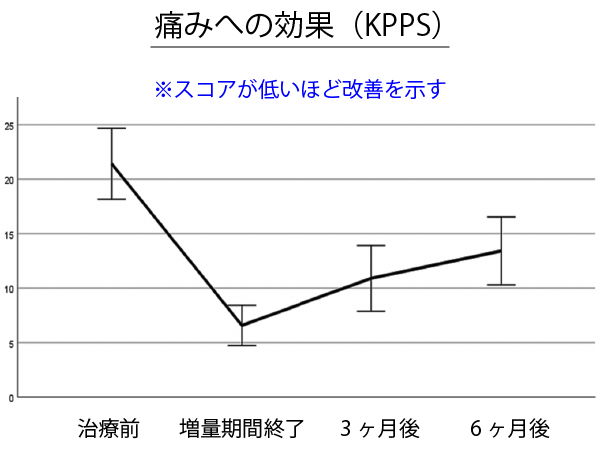
さらに、パーキンソン病特有の疼痛においても、治療前後において中程度の改善が認められました(KPPSの平均スコア:-8点・効果量:-0.55、MDS-UPDRS1.9の平均スコア:-0.74・効果量-0.74)。
一方、パーキンソン病の重症度(ホーン・ヤールの重症度分類)、運動症状(MDS-UPDRS PartⅡ・Ⅲ・運動総スコア)、不安(HADS、MDS-UPDRS1.4)、疲労度(FSS)、衝動制御障害(QUIP-RS)などにおいては、治療前後において有意な効果が観察されませんでした。
これらの結果から、著者は「結論として、ナビロンはパーキンソン病患者を対象とした長期の非盲検試験において良好な忍容性を示した。さらに、ナビロンは全般的な非運動症状、睡眠障害、疼痛を改善した」
「有効性の結果は、カンナビノイドの恩恵を受けるパーキンソン病患者のほとんどが6ヵ月後も治療反応性を維持していることを示している。我々のデータは、ナビロンがパーキンソン病患者の非運動症状の負担を軽減する有望で安全な治療薬であることを示唆している」と結論づけています。
ただし、この研究にはサンプルサイズが小さいこと、元々治療に反応があった患者を対象としたこと、治療の比較対象が存在しないこと、プラセボ効果の可能性など、いくつかの制限があります。そのため、ナビロンの有効性と安全性を実証するためには、さらなる研究が必要となります。
なお、2023年に公開されたアメリカの研究では、医療用大麻治療を受けていたパーキンソン病患者69名のうち、87%が医療用大麻の使用によりパーキンソン病症状(けいれん・ジストニア、疼痛、痙縮、食欲不振、ジスキネジア、振戦など)が改善したと回答。さらに、オピオイドを服用していた患者の56%(14名)が医療用大麻の使用後、オピオイドの中止・減薬を報告しています。