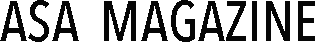CBDV(カンナビジバリン)は1969年に初めて単離されたカンナビノイドで、天然の大麻草に少量しか含まれていない「マイナーカンナビノイド」に該当します。
CBDVの発見は50年以上も前ですが、研究が進み始めたのはここ10年ほど。
CBDVはCBDと似た構造を持っており、精神活性作用はありません。そのため、CBDと同じような効果が期待されており、てんかんや自閉症スペクトラム症に対しては臨床試験も行われています。
CBDVの作用点
CBDVは基本的にCB1受容体、CB2受容体に対し親和性が低いとされています(CB2受容体に関しては高かったとする報告もあります)。
CBDは間接的にCB1受容体を活性化するとされていますが、CBDVでは現時点でまだそのようなことは明らかとなっていません。一方で、CBDVはCB2受容体を活性化させたことが報告されています。
それ以外にも、痛みやてんかんなどに関連するTPRV1を活性化し脱感作した(受容体の働きを弱める)こと、自閉症スペクトラム症やがんなど様々な疾患に関連するGPR55に対し拮抗作用したこと、てんかんの治療標的ともなっているGABAA受容体に作用したことなどが報告されています。
CBDVの効果
てんかん
CBDVは2012年の研究において、様々なてんかんモデルマウスに対し初めて抗てんかん作用を示しました。
2019年の研究では、新生児期(生後10日)のラットでは一部のてんかんにしか有効性を示さなかったものの、乳児期(生後20日)のラットでは様々なてんかんに対し有効性を示したことが報告されています。また、より幼い生後7日のラットで安全性を検証した結果、神経毒性が低いことも示されました。つまり、CBDVは乳児期のてんかんに対し安全に活用できる可能性があるということになります。
18ヶ月に渡り行われた臨床試験では、難治性てんかんを併発したレット症候群患者5名(6〜13歳)に対してCBDVを10mg/kg/日で使用した結果、3名で80%以上の発作頻度の減少が認められました(※レット症候群については後述)。
しかし、難治性の部分発作を有する成人のてんかん患者162名を対象とした8週間の臨床試験では、CBDV群(81名、400mgx2回/日)で40.5%発作が減少したものの、プラセボ群(81名)でも37.7%減少し、有意差が認められませんでした。
2013年のマウスの研究では、CBDV主体の大麻抽出物がCB1受容体を介さずに抗てんかん作用をもたらし、CBDの抗てんかん作用に対して相加的に作用することも示されました。つまりCBDVは、難治性てんかんに対し高い有効性を持つエピディオレックスの作用を高める可能性を秘めているということになります。
また、難治性てんかんを有する19歳の男性の症例報告では、抗てんかん薬と併用して、大麻の花を牛乳で煮出して作った煎じ薬を摂取することで発作の減少が認められましたが、血液を調べた結果、最も血中濃度が高かったのはTHCでもCBDでもなく、CBDVでした。
自閉症スペクトラム症・レット症候群
レット症候群は女性にのみ発症する極めてまれな発達障害で、乳幼児期から発症します。重度の知的障害、てんかん、自閉症、運動障害、自律神経障害など多彩な症状が認められますが、現時点で根治治療はなく、対症療法のみとなっています。MECP2という遺伝子の変異が原因として特定されており、この遺伝子の変異は自閉症スペクトラム症の要因としても解釈されています。
2018年の研究では、MECP2遺伝子を変異させたマウスに対しCBDVを14日間投与したところ、健康状態、社交性、脳重量の回復が認められました。これには、第3のカンナビノイド受容体とも呼ばれるGPR55への拮抗作用が関与していたことが示されています。
その翌年の研究では、MECP2遺伝子変異マウスの海馬においてCB1・CB2受容体の増加が認められていましたが、CBDVの投与によりこれらは正常化し、記憶障害の回復も認められました。ただしこれは治療というよりは、脳機能障害の発症を遅らせるものでした。
前項の「てんかん」の部分で記載したレット症候群患者5名に対する臨床試験では、全員とはいきませんでしたが、注意力、発語、表情、活動などにおいて軽度な改善が報告されました。
2019年の研究では、出生前バルプロ酸ナトリウム曝露による自閉症スペクトラム症モデルマウスの脳(海馬)において、CB1受容体の増加、エンドカンナビノイド分解酵素(FAAH、MAGL)の活発化、炎症反応が認められました。
これに対するCBDVの予防及び治療効果を検証した結果、部分的ではあるものの、20mg/kgの用量で多動性や社交性などに対し有効性が示されました。
なお、5〜18歳の自閉症スペクトラム症の子ども100名に対するCBDVとプラセボを比較した臨床試験の結果が、来年1月末に公開される予定です。
痛み・炎症
2022年に公開された研究では、CBDVには抗炎症作用があり、マウスによる検証において鎮痛作用を示したことが報告されました。さらにCBDVはモルヒネ(オピオイド)の鎮痛作用を増強するだけでなく、モルヒネによる耐性を弱めることも示されました。
しかし、HIVに関連した神経障害性疼痛を有する患者32名に対する臨床試験では、4週間に渡ってCBDV(400mg/日)を投与しても、プラセボとの有意差が認められませんでした。
なお2019年の研究では、CBDVが潰瘍性大腸炎モデルマウスの炎症を緩和し、腸内フローラを調節したことも報告されています。
これらのことから、CBDVは炎症性の疼痛に有効な可能性があると考えられます。
その他の疾患・症状
2019年のマウスの研究では、慢性の炎症、筋肉の変性・壊死、筋力低下などを主徴とするデュシェンヌ型筋ジストロフィーに対し有効性を示しており、CBDVあるいはCBDの使用により、運動機能の低下や炎症を抑制したことが報告されています。
それ以外にも前臨床試験において、制吐作用、脳梗塞後における神経保護作用、大腸がんに対する抗がん作用などが報告されています。
CBDVの安全性
研究数が少ないため断定はできませんが、全体として安全は高いとされています。
GWファーマシューティカルズが実施した人を対象とした安全性試験では、CBDV800mg/日の5日間の経口投与または5mgの静脈内投与において、忍容性は良好であったといいます。
難治性てんかんの成人患者81名がCBDV800mg/日を8週間摂取した研究においても、全体として良好な忍容性が示されました。認めれた副作用として多かったのは、下痢(25%)、傾眠(15%)、吐き気(10%)、頭痛(9%)などでした。
治療30日目を過ぎた頃に、1名で中毒症状(運動失調、眼振、うまく喋れないなど)や肝酵素の上昇、もう1名で下痢や急性腎不全が認められましたが、これらは新たな治療を行うことなく、CBDVの投与中止後数日で回復しています。
レット症候群の子ども(6〜13歳)が18ヶ月間CBDVを10mg/kg/日の用量で摂取した研究でも、CBDVと関連した副作用は傾眠とよだれのみで、重篤な副作用は認められませんでした。
つまり、CBDVは副作用を生じる可能性はあるものの、命に関わったり、新たな治療が必要になるほどの有害性はないということになります。
さらにこれらの報告は全て高用量となっているため、サプリメント程度の摂取ではより安全であると考えられます。