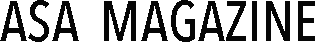脳腫瘍患者を対象とした大麻由来医薬品「サティベックス」と化学療法の併用療法による大規模な治験プログラム「ARISTOCRAT」が、遂にイギリスで開始されました。
2021年8月、リーズ大学とバーミンガム大学の研究者らは、この第2相試験(比較的少人数の患者に対する臨床試験)の実施について発表。その後、研究者らは「The Brain Tumour Charity」の募金活動を通して、45万ポンド(約7,700万円)の研究資金を調達。今月に入り、リーズ教育病院NHSトラスト(Leeds Teaching Hospitals NHS Trust)とクリスティNHSファンデーショントラスト(Christie NHS Foundation Trust)において治験を開始しました(※NHSとは、イギリス国営の保険サービスや医療サービス制度のこと)。
治験の対象となっているのは、脳腫瘍の中で最も悪性度の高い「膠芽腫(グリオブラストーマ)」を再発した患者。現在、膠芽腫に対する標準治療は手術、放射線療法、テモゾロミドによる化学療法となっていますが、5年生存率は低く、再発後の平均生存率は10ヶ月未満。しかし、現在も有望な新規治療の開発は進んでいません。
大麻に含まれる成分THCとCBDをほぼ同比率で含有したサティベックスは、膠芽腫患者27名を対象とした2021年の第1相試験(安全性や薬物動態を確認する臨床試験)において、良好な忍容性とともに、プラセボ(偽薬)と比較して1年後の生存率が高いことを示しました(サティベックス群:83%、プラセボ:44%)。
この結果を受けて今回、230名以上の膠芽腫患者を対象としたサティベックスとテモゾロミドの併用療法による臨床試験が計画され、開始に至っています。これらの患者は現在もイングランド、スコットランド、ウェールズにある14ヶ所の国営病院で募集中。なお、研究は3年間行われる予定です。
現在、サティベックスは多発性硬化症の痙縮のみに適応されており、NHSの保険適用となっています。今回の治験が成功すれば、サティベックスはテモゾロミド以来の新たな神経膠芽腫治療薬として承認され、今後NHSの保険適用となる可能性があります。
本研究の代表者であるリーズ大学臨床腫瘍学・神経腫瘍学教授スーザン・ショート(Susan Short)氏は「私たちは、ここリーズでこの臨床試験を開始できることを大変嬉しく思っています。そして、カンナビノイドベースの薬剤が最も悪性度の高い脳腫瘍の治療に役立つかどうかを知ることができるこの試験を実施することを非常に楽しみにしています。膠芽腫の治療は非常に困難です。手術、放射線治療、化学療法を行っても、ほぼすべての脳腫瘍が1年以内に再増殖してしまいます。残念ながら、このような事態に陥った場合、患者さんにとって選択肢はほとんどありません」
「カンナビノイドベースの薬剤は脳内でよく知られている作用があり、長い間、様々ながんに対する使用において関心が持たれていました。膠芽腫は、細胞表面にカンナビノイドに対する受容体を有しています。また、膠芽腫細胞を用いた実験室の研究では、これらの薬剤が腫瘍の成長を遅らせ、テモゾロミドと併用すると特に効果的であることが示されています」
「私たちは今、これらの実験室での結果と第1相試験で得られた結果をもとに、この薬剤が膠芽腫患者の延命に役立つかどうかを、世界初のランダム化臨床試験で調査する機会を得ました」とコメント。
研究を支援する慈善団体「The Brain Tumour Charity」の最高科学責任者(CSO)であるデイビット・ジェンキンソン(David Jenkinson)氏は「イギリスで実施されるこの世界初の試験が、この壊滅的な病気に対する治療を加速させることを心から期待しています。ここ10年間、膠芽腫を治療するカンナビノイドの可能性について、患者と研究者の両方から大きな関心が寄せられています」
「初期の段階で得られた知見は、本当に有望なものでした。私たちは今、化学療法にナビキシモルス(サティベックス)を加えることで、膠芽腫と診断された人々のQOLを改善し、延命に役立てられるかどうか理解することを楽しみにしています。これにより、膠芽腫の治療薬として15年以上ぶりの新薬が登場することを期待しています」と述べています。
神経膠芽腫に対するカンナビノイドの臨床報告は、すでにいくつか存在します。
オーストラリアの研究者らは2021年、手術不能な進行性の神経膠腫患者88名(このうち、91.3%が神経膠芽腫)を対象とした大麻抽出物の臨床試験を実施。この研究は、今年ロンドンで開催された国際学術集会でもシェアされています。神経膠腫患者はTHC:CBD=1:1(THC4.6mg/ml、CBD4.8mg/ml)、あるいはTHC:CBD=4:1(THC15mg/ml、CBD3.8mg/ml)を含むオイルを12週間摂取することで、一部で腫瘍の縮小や生存率の延長を認め、QOLの向上を報告しています。
オーストリアの研究者らによって報告されたケースシリーズでは、膠芽腫患者9名が標準治療に加えCBD(400mg/日)を摂取した結果、平均生存率は22.3ヶ月となり、1名を除く8名が論文公開に至るまで生存していたことが報告されています。
なお、大麻由来医薬品における新たな動きは、サティベックス以外でもみられています。
世界トップレベルの大学として知られるイギリスのオックスフォード大学は今年2月、一部の難治性てんかんに使用されている高濃度CBD製剤「エピディオレックス」を用いて、統合失調症などの精神病に対する有効性を検証する大規模な国際的治験を年内に開始することを発表しています。
The Brain Tumour Charity「ARISTOCRAT – a pioneering trial using a cannabinoid-based drug to treat brain tumours」https://www.thebraintumourcharity.org/media-centre/news/research-news/aristocrat-a-pioneering-trial-using-a-cannabinoid-based-drug-to-treat-brain-tumours/
University of Birmingham「Cannabinoid-based drug trial for brain tumours begins」https://www.birmingham.ac.uk/news/2023/cannabinoid-based-drug-trial-for-brain-tumours-begins
University of Birmingham「ARISTOCRAT: A randomised controlled phase II trial of temozolomide with or without cannabinoids in patients with recurrent glioblastoma」https://www.birmingham.ac.uk/research/crctu/trials/aristocrat/index.aspx
Cannabis Health News「World-first trial of cannabis-based drug in brain tumours launches in UK」https://cannabishealthnews.co.uk/2023/05/11/world-first-trial-of-cannabis-based-drug-in-brain-tumours-launches-in-uk/