8月16日、大麻成分THCとCBDを同比率で含有したオイルを制吐剤と併用することで、抗がん剤の副作用である悪心・嘔吐がより効果的に緩和されたことがタイの研究チームによって報告されました。論文は「International Journal of Women’s Health」に掲載されています。
抗がん剤に代表される副作用として、悪心・嘔吐があります。これは抗がん剤により、脳の延髄と呼ばれる場所にある「嘔吐中枢」が刺激されるために生じるとされています。
抗がん剤が嘔吐中枢を刺激する経路は複数存在。まず、抗がん剤は腸の細胞からセロトニンを分泌させ、迷走神経を介して脳の嘔吐中枢を刺激します。また、抗がん剤は脳にある「化学受容器引き金帯(CTZ)」と呼ばれる部位を直接刺激することでも嘔吐中枢を刺激します。
さらに、抗がん剤は脳において「サブスタンスP」と呼ばれる物質を放出させます。この物質は嘔吐中枢と化学受容器引き金帯にある「ニューロイキン1(NK1)受容体」に作用することで、嘔吐中枢を刺激します。
これらが原因となって悪心・嘔吐が出現することになりますが、抗がん剤による悪心・嘔吐には以下の4種類があります。
急性悪心・嘔吐:抗がん剤投与後24時間以内に出現。
遅発性悪心・嘔吐:抗がん剤投与後24時間〜1週間程度で出現。
突出性悪心・嘔吐:制吐剤の予防投与を行っても突発的に出現。
予期性悪心・嘔吐:以前抗がん剤で悪心・嘔吐を経験したことから、次の抗がん剤治療前に精神的な要因で出現。
現在では「セロトニン5-HT3受容体拮抗薬」の登場により、抗がん剤による悪心・嘔吐はだいぶ軽減できるようになっています。遅発性嘔吐に対しては「NK1受容体拮抗薬」も有効です。
これらの予防投与で有効性が認められない「予期性悪心・嘔吐」には、デキサメタゾンと呼ばれる「副腎皮質ステロイド」が用いられます。精神的要因で発症する予期性悪心・嘔吐には「ベンゾジアゼピン系抗不安薬」などが使用されます。
抗がん剤による悪心・嘔吐と大麻
セロトニン5-HT3受容体拮抗薬が登場する前の1980年代、アメリカのFDA(食品医薬品局)は抗がん剤による悪心・嘔吐の制吐剤として、大麻由来医薬品であるドロナビノールやナビロンを承認しています。
このような長い歴史もあり、抗がん剤による悪心・嘔吐に対する医療用大麻のエビデンスは数多く蓄積されていますが、最近のものも含めほとんどのシステマティックレビューでは、医療用大麻は標準的な制吐剤よりも有効性が劣るため、第一選択薬とはならないと結論づけられています。
とはいえ、医療用大麻が合法な国や州の多くは、抗がん剤による悪心・嘔吐に対し標準的な制吐剤で有効性が認められない場合に、医療用大麻の使用を認めています。
大麻や大麻に含まれる有効成分「カンナビノイド」は、主にECS(エンドカンナビノイドシステム)と呼ばれる神経系に作用することで様々な医療効果が認められるとされています。大麻による制吐作用のメカニズムはまだ明らかにされていませんが、主にECSの構成要素の1つである「CB1受容体」の活性化が関連していると考えられています。
CB1受容体を活性化する成分には、私たちの体内で作られるアナンダミドや2-AGといったエンド(内因性)カンナビノイドや、大麻に含まれる主なカンナビノイドであるTHCなどが挙げられます。大麻に含まれるもう1つの主なカンナビノイドであるCBDは、CB1受容体の働きを弱める一方、体内のアナンダミド量を増やすことで知られています。
トガリネズミを用いた研究では、CB1受容体拮抗薬の投与により用量依存的に嘔吐が誘発される一方、CB1作動薬やTHCは制吐作用を発揮。同じくトガリネズミを用いた2009年の研究では、THCが抗がん剤による急性及び遅発性悪心・嘔吐の両方に制吐作用をもたらしましたが、この作用はCB1受容体拮抗薬により消失しています。
CB1受容体とセロトニン5-HT3受容体は脳の様々な場所で共発現しており、THCやアナンダミドはこれらの受容体の相互作用を介して制吐作用をもたらすとも言われています。
2010年の研究では、CBDもセロトニン5-HT3受容体の働きを邪魔するような作用を示しています。他にも、CBDは自己受容体であるセロトニン5-HT1A受容体を活性化することでセロトニンの分泌量を減らす可能性があり、これが制吐作用に関連するとも推測されています。
実際に2012年の研究では、CBDは抗がん剤によって悪心・嘔吐を誘発したトガリネズミに制吐作用をもたらしましたが、この作用はセロトニン5-HT1A受容体拮抗薬により消失しています。
THCでは他にも、抗がん剤により悪心・嘔吐を誘発したトガリネズミにおいてサブスタンスPの放出を抑制し、用量依存的に制吐作用を発揮。この作用はCB1受容体拮抗薬及び逆作動薬、そしてNK1受容体拮抗薬により消失しています。
タイの婦人科がん患者を対象とした臨床試験
タイの研究チームは抗がん剤による悪心・嘔吐に対する大麻オイルの有効性を評価するため、中程度〜高度の催吐作用を有する抗がん剤治療を受ける予定の婦人科がん患者を対象とした臨床試験を実施。
研究を完了した参加者は54名で、平均年齢は54.4歳。59.3%が進行がんで、卵巣がん22名、子宮内膜がん12名、子宮頸がん16名、その他4名。全員が「プラチナ製剤」と呼ばれる抗がん剤(カルボプラチンまたはシスプラチン)による治療を受けました。
また、参加者は全員、抗がん剤投与の30分前にデキサメタゾン(ステロイド)、オンダンセトロン(セロトニン5-HT3受容体拮抗薬)、ラニチジン(ヒスタミンH2受容体拮抗薬)といった標準的な制吐剤の投与を受けることに同意しました。
使用された大麻オイルは、THCとCBDを1:1の割合で含有した国営製薬公社(GPO)の製品(1mlあたりTHC2.7mg、CBD2.5mg)です。
参加者はランダムにA群とB群に分けられ、A群では抗がん剤治療の第1クール目で大麻オイル、第2クール目でプラセボ(偽薬)を使用。B群ではこの逆の順番で投与が行われました。第1クールと第2クールの間には少なくとも21日間の期間がありました。
大麻オイル及びプラセボは、1〜3日目では朝食前と夕食前に1滴ずつ、4〜5日目では朝・昼・夕食前に1滴ずつ舌下投与。
制吐作用の評価は、参加者が11段階で自己評価することにより行われました(0=吐き気なし、10=最悪の吐き気)。
有効性をできるだけ正確に評価するため、治験を担当した医師と患者はどの薬を服用しているか分からないように工夫されました(二重盲検クロスオーバー比較試験)。
大麻オイルの併用で吐き気が有意に軽減
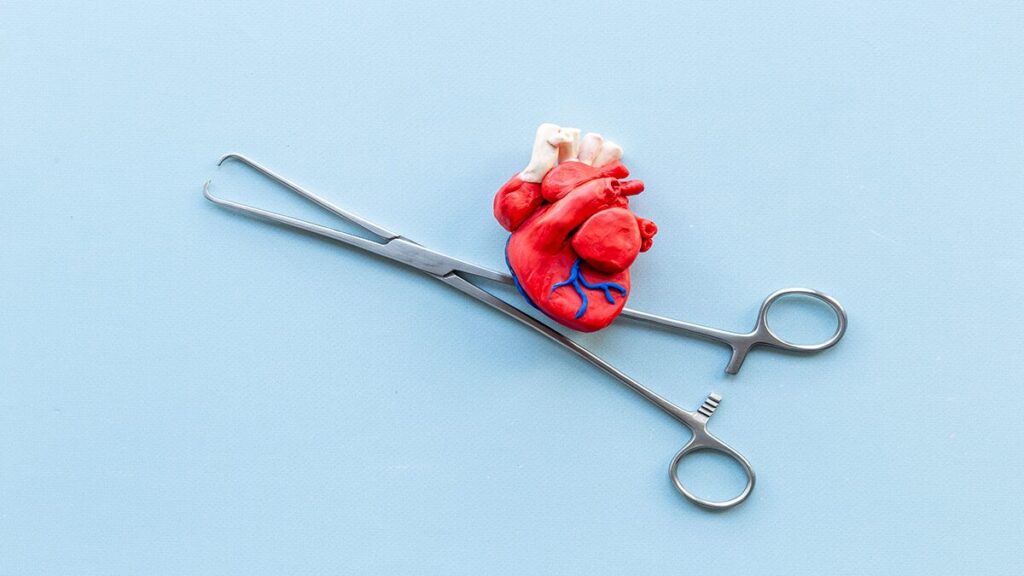
研究の結果、悪心・嘔吐の平均スコアは大麻オイルで2.1(1日目:2.0、2日目:2.2、3日目:2.4、4日目:2.1、5日目:1.8)、プラセボで3.0(1日目:3.1、2日目:3.0、3日目:3.0、4日目:2.7、5日目:3.2)となり、大麻オイルで有意に低くなりました。
A群では第1クールでスコアが低かったものの、第2クールではスコアが上昇。B群では第1クールでスコアが高かったものの、第2クールでスコアが減少しており、大麻オイルの有効性が示されました。
大麻オイルの副作用として最も多く報告されたのはめまいと鎮静(51.8%)。それ以外の副作用では、大麻オイルとプラセボで報告数に有意差が認められませんでした。
大麻オイルは抗がん剤による悪心・嘔吐の緩和を補助
今回の研究では標準的な制吐剤の服用もあり、全体として悪心・嘔吐のスコアは低くなっていたものの、大麻オイルを使用したクールでは有意にスコアが減少(改善)していました。
研究者らはより多くの患者を対象とした臨床試験が必要としながらも、催吐性の高い抗がん剤治療を受けた婦人科がん患者の悪心・嘔吐において、THC:CBD=1:1の大麻オイルは「適切な補助薬である」と結論づけています。
他にも、2020年のオーストラリアの臨床試験では、以前抗がん剤による悪心・嘔吐で制吐剤が効かなかった患者に、THC:CBD=1:1の経口カプセル(1カプセル=THC2.5mg、CBD2.5mg)を1日3回2〜4カプセルずつ服用してもらった結果、プラセボと比較して25%で完全奏効が認められ、1日の最大嘔吐回数や悪心・嘔吐の自己評価尺度においても有意な改善が認められています。
慎重な判断を要する
これらの結果は有望ではありますが、以下のことを考慮し、慎重に判断する必要があります。
まず、CBDは試験管内の研究において、今回の研究で使用されたプラチナ製剤の作用を減弱させる可能性が指摘されています。
ポーランドの研究チームは昨年、CBDとミトキサントロン(トポイソメラーゼ阻害薬)では相加的な相互作用が認められたのに対し、CBDとシスプラチンでは拮抗作用が認められたことを報告。
チェコの研究者らは最近、CBDとCBGがシスプラチン、オキサリプラチン、カルボプラチンといったプラチナ製剤の抗がん作用を減弱させたことを報告。このためにこれらのカンナビノイドは抗がん剤による副作用を緩和するとまで指摘しています。
一方で、THCではこのような拮抗作用が認められないという結果に。そのため、研究者らはCBDを含有した大麻オイルをプラチナ製剤と併用するべきではないと警告し、ドロナビノールのようなTHC製剤を選択すべきだと述べています。
つまり、がんと闘うために抗がん剤を使用しているにも関わらず、カンナビノイド(特にCBD)は一部の抗がん剤の効果を弱めてしまう危険性があるということです。試験管内の研究であるため断定はできませんが、今後の研究結果を注視する必要があります。
また、抗がん剤による悪心・嘔吐に有効性を示しているのは主に大麻由来医薬品や標準化された大麻製品であるため、嗜好用として流通している大麻では異なる結果になる可能性があります。
大麻やカンナビノイドは適量では医療効果を発揮しますが、それ以外の量では効果がなかったり、逆に病状を悪化させることで知られています(二相性)。
特に、過剰な大麻の使用は嘔吐に対する身体反応を混乱させ、「カンナビノイド嘔吐症候群(CHS:Cannabis Hyperemesis Syndrome)」を引き起こすことで有名です。
カンナビノイド嘔吐症候群は初期段階では腹部の不快感、食欲不振、吐き気などを認めますが、食生活に大きな影響はありません。しかし、増悪すると反復性の嘔吐や腹痛を認め、脱水、栄養失調、電解質バランス異常を始めとした数々の合併症リスクが生じるため、医療機関への受診を要します。
カンナビノイド嘔吐症候群の治療として一番有効なのは、原因となっている大麻の使用をやめること。他にも、制吐剤、ハロペリドールやドロペリドールなどのドーパミン受容体拮抗薬、カプサイシン(TRPV1受容体の活性化)などが有効とされています。